Меню
Соціальні мережі
Розділи
«Молнупіравір»: що відомо про пігулки від COVID-19
16087
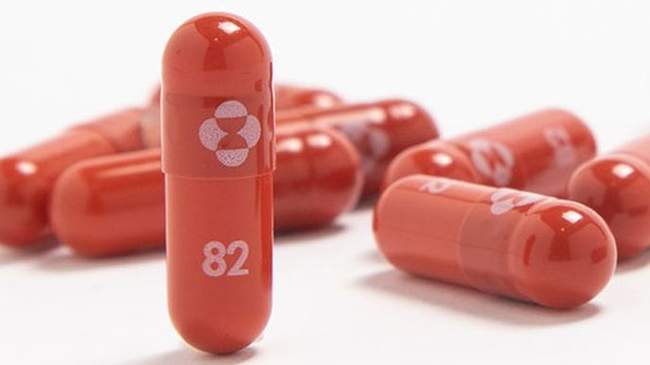
Сьогодні, 26 січня, МОЗ України зареєструвало препарат для лікування COVID-19 «Молнупіравір» для екстреного застосування.
«Молнупіравір» планують використовувати для інфікованих людей, які знаходяться у групах ризику, щоб убезпечити їх від переходу із легкого ступеня тяжкості захворювання до середнього та важкого.
«Ми почали готуватися до чергової хвилі ковіду завчасно. Тому ще минулого року розпочали перемовини щодо закупівлі 300 тис. курсів препарату "Молнупіравір", – зазначив перший заступник міністра охорони здоров’я Олександр Комаріда. – Нині МОЗ завершило реєстрацію препарату, тому очікуємо його постачання найближчим часом».
Що таке «Молнупіравір»?
«Молнупіравір» — це противірусний препарат, що запобігає середнім, тяжким та летальним захворюванням на COVID-19.
Препарат був розроблений в Університеті Еморі університетською компанією з розробляння інноваційних препаратів «Drug Innovation Ventures at Emory» (DRIVE). Пізніше права на нього придбала компанія «Ridgeback Biotherapeutics», що базується в Маямі, яка згодом співпрацювала з «Merck & Co.» у подальшому дослідженні та маркетингу препарату.
«Молнупіравір» спочатку розробляли як противірусний препарат для лікування грипу. Він вбудовується в РНК вірусу, викликає мутації в вірусній РНК і у такий спосіб зупиняє його реплікацію (самовідтворення).
Випробування препарату показали, що він удвічі знижує ймовірність госпіталізації або смерті при захворюванні COVID-19. Із групи пацієнтів, які отримували препарат, лише 7,3% були госпіталізовані після 29 днів з початку випробування (при цьому не було зафіксовано жодної смерті). Водночас як серед пацієнтів, які отримували плацебо, відсоток госпіталізацій і смертей досяг 14,1% (було зафіксовано 8 летальних випадків), тобто був удвічі вищим.
В який країнах використовується?
У червні 2021 року Міністерство охорони здоров'я та соціальних служб США зобов'язалося закупити препарат на суму 1,2 мільярда доларів США (відповідає приблизно 1,7 мільйонам повних курсів препарату) у виробника, компанії Merck, якщо препарат отримає дозвіл на екстрене використання (EUA) або схвалення Управління контролю за продуктами та ліками США (FDA).
У жовтні 2021 року Комітет з лікарських засобів людини (CHMP) Європейського агентства з лікарських засобів (EMA) розпочав безперервний огляд «Молнупіравіру».
У листопаді 2021 року «Молнупіравір» був схвалений у Великій Британії Агентством з регулювання лікарських засобів та товарів медичного призначення (MHRA) для лікування підтверджених інфекцій COVID-19. MHRA видало умовний дозвіл на продаж, дійсний у Сполученому Королівстві, та дозвіл на використання у надзвичайних ситуаціях для Північної Ірландії. Згідно з угодою, підписаною у жовтні, Великобританія розраховує отримати 480 тис. доз «Молнупіравіру» у 2022 році.
Австралія купила 300 тис. курсів. У жовтні 2021 року новозеландський фармацевтичний постачальник Pharmac закупив 60 тис. доз.
У листопаді 2021 року Генеральне управління з лікарських засобів Бангладеш (DGDA) затвердило дозвіл на продаж «Молнупіравіру», виробленого Beximco Pharmaceuticals та Eskayef Pharmaceuticals під торговими марками Emorivir та Monuvir відповідно.
Сінгапур та Південна Корея також уклали угоди про купівлю. Merck вже ліцензувала цей препарат п’яти виробникам генериків в Індії.
Як діє «Молнупіравір»?
У листопаді Кабмін додав «Молнупіравір» та «Ритонавір» до переліку засобів, які використовують для лікування COVID-19.
Цей противірусний препарат знижує здатність коронавірусу реплікуватися в клітинах організму, тим самим уповільнюючи розвиток COVID-19.

На основі даних 775 пацієнтів, які взяли участь у дослідженні й приймали «Молнупіравір», було встановлено таке:
- госпіталізовані 7,3% пацієнтів,
- із пацієнтів, які приймали плацебо, госпіталізовані 14,1%,
- серед тих, хто приймав експериментальні ліки, ніхто не помер,
- із пацієнтів, яким давали плацебо, восьмеро померли.
Ці дані були оприлюднені у пресрелізі компанії і поки що не були підтверджені незалежними рецензіями.
Судячи з результатів дослідження, для ефективної дії «Молнупіравір» необхідно вживати на перших етапах появи симптомів. Раніше виробники намагалися провести ще одне дослідження за участю пацієнтів, яких госпіталізували з важкими симптомами коронавірусу, але його довелося припинити, оскільки препарат відчутних результатів не приносив.
Перевага пігулок у тому, що їх можна без проблем приймати вдома. Інші ліки, наприклад, противірусний препарат Remdesivir, необхідно вводити внутрішньовенно. Окрім того, таблетки, зазвичай, легко виробляти, транспортувати, зберігати та застосовувати. Це робить їх особливо привабливим варіантом для країн з низьким та середнім рівнями прибутку, слабкою інфраструктурою та обмеженими поставками вакцин.
Нагадаємо, 22 січня міністр охорони здоров'я Віктор Ляшко повідомив, що в Україні буде зареєстрований препарат «Молнуправір» - таблетки від коронавірусу. МОЗ попередньо вже законтрактував 300 тисяч доз препарату, реєстрація очікується наступного тижня.
Фото: Українська правда